摘要:文章为某网络整理而成,主要讲述上海金山生活污水处理企业-低温含铁锰氨地下水中氨去除影响研究,含铁锰氨地下水在我国东北地区广泛分布, 含铁锰氨地下水生物净化工艺能够实现铁锰氨的净化去除, 在此工艺中铁的氧化耗氧量为......
关键词:生物,生活污水处理,上海金山生活污水处理企业.
上海金山生活污水处理企业为您整理热点:低温含铁锰氨地下水中氨去除影响研究。
含铁锰氨地下水在我国东北地区广泛分布, 含铁锰氨地下水生物净化工艺能够实现铁锰氨的净化去除, 在此工艺中铁的氧化耗氧量为0.143 mg·L-1, 锰的氧化耗氧量为0.29 mg·L-1, 而氨氮的氧化耗氧量高达4.57 mg·L-1, 并且随着近年来地下水中氨氮浓度的不断升高, 势必会大幅增加水中DO(溶解氧)的消耗, 导致原水中原本紧张的DO更加不足, 使供需矛盾加剧.有研究发现氨氮经过全程自养脱氮(completely autotrophic ammonium removal over nitrite, CANON)过程氧化耗氧量仅为1.94 mg·L-1, 由此可知, 当进水中的氨氮通过CANON过程去除时, 会降低水中溶解氧的消耗, 从而提升出水中的溶解氧, 提高生物滤柱的抗冲击负荷.因此CANON工艺引起了研究者的广泛关注.梁雨雯等实现了常温条件下铁锰氨复合污染地下水耦合自养脱氮过程, 李冬等成功启动并运行了低温生物除铁锰硝化耦合CANON工艺.
在生物除铁锰硝化耦合CANON工艺中, 提高CANON过程去除的氨氮能够降低水中DO的消耗, 提高生物滤柱的抗冲击负荷.有研究表明在氨氮仅通过硝化作用去除的生物滤柱中提升滤柱运行滤速不仅会导致滤料表面的水流剪切力增大, 降低硝化细菌对DO等基质的网捕效率, 并且会缩短滤柱的EBCT(空床接触时间), 导致硝化反应时间减少进而使硝化作用对氨氮的去除率降低.故由上述可知, 滤速增加会影响氨氮仅通过硝化作用去除的生物滤柱中氨氮的去除, 而为明晰在生物除铁锰硝化耦合CANON工艺中滤速对氨氮去除的影响, 本实验在出水合格的情况下梯次调节滤柱的运行滤速, 探究不同进水浓度时滤速对硝化作用及CANON过程的影响.鉴于此, 笔者在东北某地水厂运行了生物除铁锰硝化耦合CANON工艺, 探究滤速对低温含铁锰氨地下水中氨去除的影响, 并以此分析水质对低温含铁锰氨地下水中氨去除的影响.
1 材料与方法
1.1 实验装置
采用中试装置在净化车间开展低温生物除铁锰硝化耦合CANON工艺实验研究.装置采用已停止运行1个月的成熟生物滤柱.如图 1所示, 由有机玻璃制成, 高为3 000 mm, 内径为200 mm.滤柱采用装填总高度为1 600 mm的双层滤料, 上层400 mm为级配为1.0~1.2 mm的无烟煤成熟滤料, 下层1 200 mm为级配为0.6~1.2 mm的锰砂滤料, 承托层采用级配为1.2~20.0 mm的鹅卵石, 厚度为400 mm.
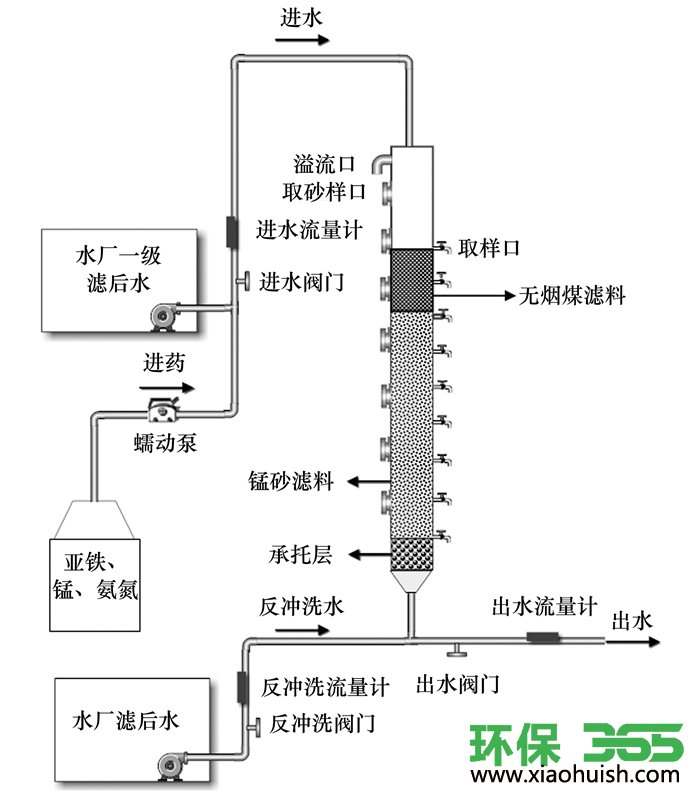
图 1 反应装置示意
1.2 水质与检测方法
以水厂两级生物净化工艺中的一级滤池滤后水与硫酸亚铁(FeSO4)、硫酸锰(MnSO4)及硫酸铵[(NH4)2SO4]配置成的混合液作为实验进水.主要水质指标如下:水温6~8℃, Fe(Ⅱ) 2.91~6.35 mg·L-1, Mn(Ⅱ) 0.47~0.98 mg·L-1, NH4+-N 1.15~2.26 mg·L-1, NO2--N痕量, NO3--N 0.07~0.34 mg·L-1, 高锰酸盐指数痕量, pH为6~7, DO为8.3~10.0 mg·L-1.
Fe(Ⅱ):二氮杂菲分光光度法, Mn(Ⅱ):过硫酸铵分光光度法, NH4+-N:纳氏试剂比色法, NO2--N:N-(1-萘基)-乙二胺光度法, NO3--N:紫外分光光度法, 化学需氧量:高锰酸盐指数(酸法), pH、DO和水温:便携式测定仪(Qxi 315i-WTW).
1.3 实验方法
实验前向滤柱中接种1 L运行稳定的CANON污泥上清液, 并以0.5 m·h-1循环培养3 d后, 以2.0 m·h-1的滤速启动滤柱.当满足1<ΔNH4+-N(氨氮变化量)/ΔNO3--N(硝氮变化量)<8且连续稳定时, 即表明硝化耦合CANON工艺启动成功, 启动成功后出水达标并稳定超过7 d, 即视为滤柱在此条件下运行成功, 而后逐步调节进水浓度及滤速, 探究滤速与水质对低温含铁锰氨地下水中氨去除的影响.
1.4 硝化耦合CANON工艺分析方法
本实验过程中对进出水铁锰、“三氮”(氨氮、硝氮、亚氮)、DO进行检测.根据氮素守恒关系分析生物滤柱中氨氮转化去除途径, 氮素守恒关系式如下(1)~(6)所示[8].

式中, Δ(NH4+-N):进出水氨氮变化量, (NH4+-N)in:进水氨氮量, (NH4+-N)out:出水氨氮量; Δ(NO2--N):进出水亚氮变化量, (NO2--N)out:出水亚氮量, (NO2--N)in:进水亚氮量; Δ(NO3--N):进出水硝氮变化量, (NO3--N)out:出水硝氮量, (NO3--N)in:进水硝氮量; TN:氮素总量, TNin:进水氮素总量, TNout:出水氮素总量, TNloss:进出水氮素损失, 上述参数的单位均为mg·L-1; NLR为氮素损失率(%).
1.5 滤料吸附性能分析
参考前人研究[8], 具体为:分别在滤柱的20、40、80、120和160 cm处的取砂样口取5 g滤料, 并将滤料用去离子水清洗干净后, 置入高压灭菌器(新华LMQ.C型立式灭菌器)中, 以120℃灭活2 h后取出备用.分别称取0.1 g上述不同位置的灭活滤料, 并分别放入500 mL具塞锥形瓶中进行氨氮吸附实验.在锥形瓶中分别加入250 mL浓度为1.5 mg·L-1的NH4+-N溶液, 以100 r·min-1的转速在25℃的条件下恒温振荡12 h后, 取上清液并用0.45 μm的滤膜过滤后测试溶液剩余的氨氮浓度, 并重复实验2次.
2 结果与讨论
2.1 生物滤柱启动
2.1.1 培养中铁锰的净化能力
图 2为运行过程中铁锰浓度变化情况.由于亚铁在滤柱中主要是通过化学接触氧化作用去除的, 所以滤柱在启动初期就表现出良好的除铁性能, 在整个过程中滤柱的除铁性能并未受滤速及浓度的影响, 出水总铁均能满足《生活饮用水卫生标准》(GB 5749-2006)中的限值要求.而锰在滤柱中主要是通过生物作用去除的, 且有研究表明, 滤柱短期停运对于生物滤层除锰效果的影响是轻微的, 正如图 2所示在滤柱启动初期出水锰浓度不达标, 此后仅经过10 d的培养, 出水锰浓度便逐渐降低至0.09 mg·L-1, 此后出水锰浓度均能满足标准中的限值要求, 生物除锰启动成功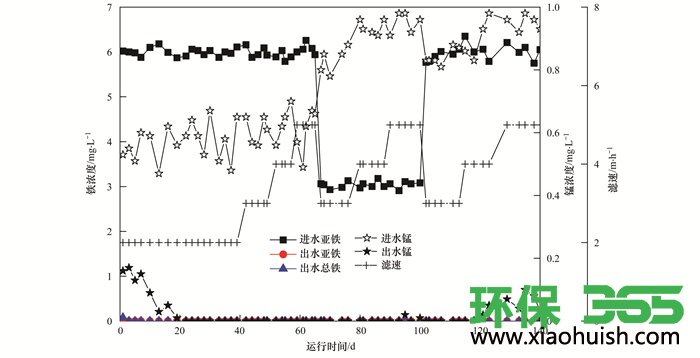
图 2 运行过程中铁锰浓度变化
2.1.2 培养中氨氮的净化能力
图 3为运行过程中进出水“三氮”变化情况.由图 3(a)知, 启动初期滤后水氨氮浓度首先升高, 造成此现象的原因是滤料具有物理吸附作用, 然而其吸附位是有限的, 故随着运行时间的延长, 滤料的吸附能力逐渐饱和, 滤柱对氨氮的吸附能力逐渐降低, 故滤柱在启动初期出水氨氮浓度表现出增加的趋势.由图 3(b)知, 启动的前30 d, 出水亚氮浓度高于进水, 表明滤柱中的AOB菌(氨氧化菌)活性或生物量强于NOB(亚硝酸盐氧化菌)和AnAOB(厌氧氨氧化菌), 出水亚氮得到了积累.分析图 3(c)可知, 在滤柱启动初期, 出水硝氮浓度明显高于进水硝氮浓度, 表明停运1个月的生物滤柱经过短时间培养后仍然具有较好的硝化性能, 随着生物滤柱的培养, 出水硝氮浓度逐渐升高.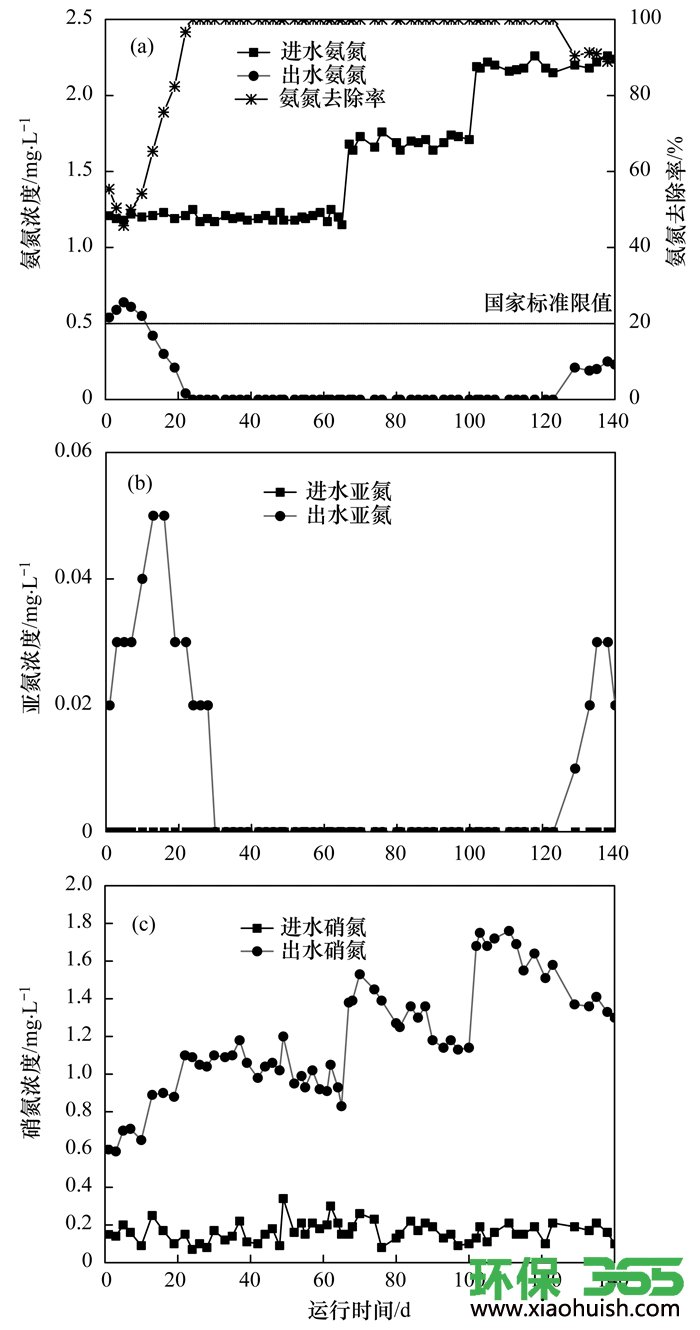
图 3 运行过程中“三氮”变化
2.1.3 培养中进出水总氮变化
进出水“总氮”变化如图 4所示.在启动初期, 出水总氮浓度低于进水总氮浓度, 总氮浓度不守恒, 导致滤柱在启动初期总氮浓度不守恒的主要原因是滤料通过物理吸附作用对水中的氨氮和硝氮进行了吸附, 导致水中的总氮浓度降低.随着滤料物理吸附作用的逐渐饱和, 滤料吸附水中氨氮和硝氮的量逐渐降低, 而此时滤柱中AnAOB的活性和生物量并未完全恢复, 因此, 滤柱中的总氮损失逐渐降低.在滤料对氨氮吸附达到饱和的过程中, 更高负荷的氨氮进入滤层深处, 微生物能够接触到更多的氨氮, 提高了其对氨氮的网捕效率, 微生物与氨氮所处的动态平衡遭到破坏, 滤料表面AOB、NOB和AnAOB不断富集, 微生物历经第一活性增长期, 去除氨氮的生物效能逐渐增强.随着AnAOB的生物量及生物活性的提高, ANAMMOX过程将逐渐建立, 总氮损失会进一步升高并趋于稳定.
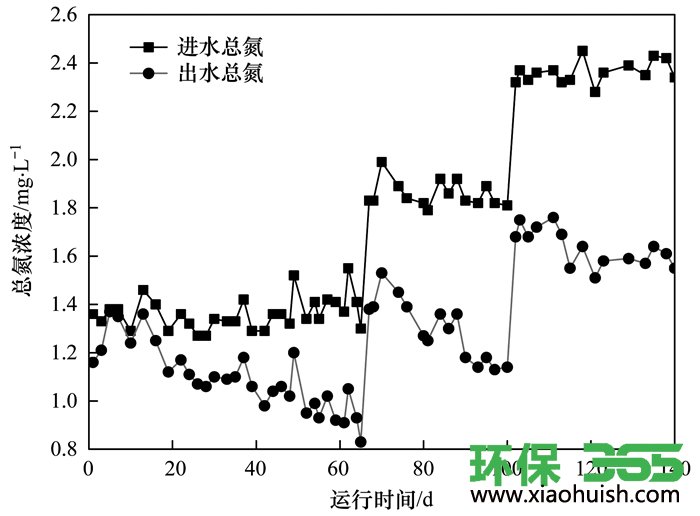
图 4 进出水“总氮”变化
2.1.4 NLR及特征值分析
有研究表明, 当溶解氧一定时氨氮的CANON过程分为两个步骤:①在生物膜外的好氧环境中, NH4+-N被AOB氧化成NO2--N; ②NH4+-N和上过程产生的NO2--N经过扩散作用进入到生物膜内的缺氧环境中, 在AnAOB的作用下两者发生反应从而得到去除, 反应式如式(7)所示.
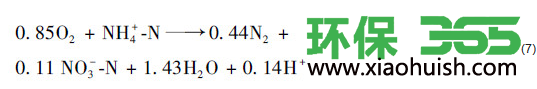
分析式(7)可知, 若氨氮全部经过CANON作用去除, 则滤柱中ΔNH4+-N与ΔNO3--N的理论比值应为8, 若1<ΔNH4+-N/ΔNO3--N<8且连续稳定, 即表明成功启动硝化耦合CANON工艺.图 5为滤柱运行过程中NLR和特征值变化情况, 在启动初期由于滤料的物理吸附作用, 导致滤柱中TNloss(氮素损失)较多, NLR较高.由图 3(c)知, 滤柱在启动初期就具有硝化能力, 出水中硝氮浓度大于进水硝氮浓度, 并且滤柱同样可以吸附水中的硝氮, 因此ΔNH4+-N大于ΔNO3--N, 特征值>1.由于滤料的吸附位是有限的, 故随着滤柱的运行, 滤料的吸附能力逐渐降低, 生物去除氨氮的能力增强, 所以NLR和特征值逐渐降低.随着滤料吸附趋于饱和以及ANAMMOX过程的逐渐建立, NLR和特征值将逐渐升高并趋于稳定.
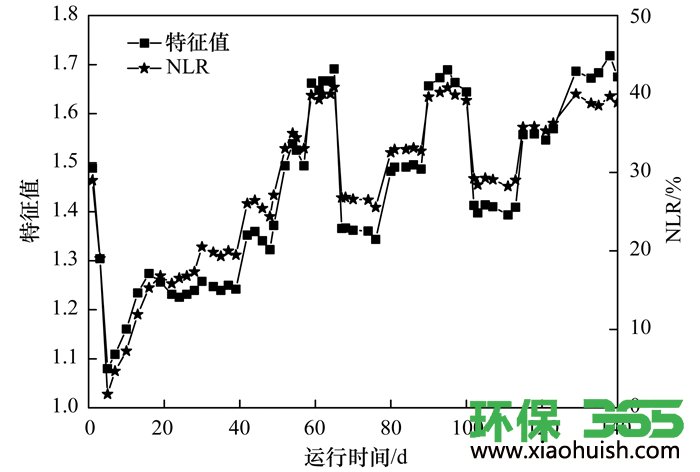
图 5 运行过程中氮素损失率与特征值的变化
在滤柱运行至27 d和39 d时分别取20、40、80、120和160 cm处的滤料, 经高温灭菌后进行吸附性能分析实验, 由表 1分析知, 原氨氮浓度为1.500 mg·L-1, 各处滤料吸附后氨氮浓度均约为1.500 mg·L-1, 故滤料在27 d时已经吸附饱和, 此后滤柱中的氮素损失与滤料的吸附作用无关, 而是由ANAMMOX过程造成的.结合图 5分析知, 滤柱在39 d时特征值约为1.24, 在1<ΔNH4+-N/ΔNO3--N<8的理论范围内, 且连续稳定.因此, 低温生物除铁锰硝化耦合CANON工艺经过40 d的培养启动成功.
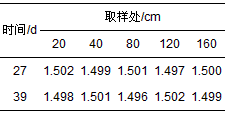
表 1 滤料吸附实验分析/mg·L-1
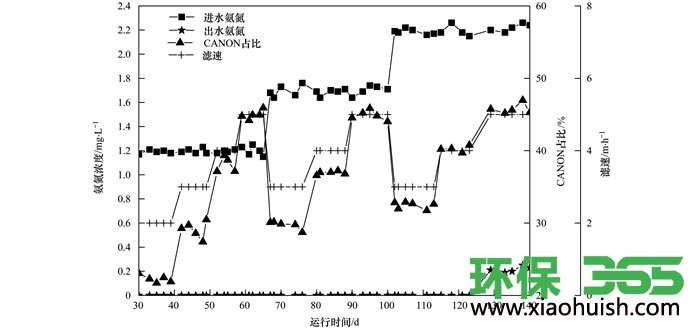
图 6 运行过程中CANON占比变化
2.2 滤速与水质对氨氮去除的影响分析
本实验采用氮素守恒计算模型对氨氮转化去除路径进行分析.由表 1成熟滤料吸附实验分析知, 27 d时滤料已吸附饱和, 可忽略滤料对氨氮转化去除的影响; 此外滤柱进水中高锰酸盐指数痕量, 故异养反硝化不能得到足够的电子受体, 因此亦忽略其对氮素转化去除的影响; 且在生物滤柱培养成熟后, 微生物的同化作用始终处于动态平衡状态对于氮素转化去除的贡献少于5%, 因此模型计算时并未考虑.综上所述, 分析认为在此生物滤柱中总氮损失仅是由CANON作用造成的, 参照前人研究采用式(7)及式(8)对CANON作用和硝化作用去除氨氮占比进行计算.
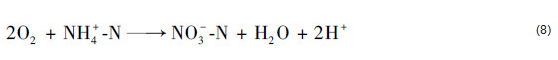
设硝化作用和CANON作用去除的氨氮分别为x和y, 则可得式(9)及式(10):
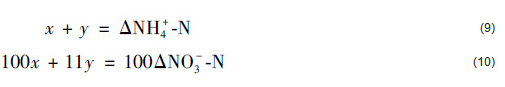
由上可得, CANON作用去除的氨氮占比为:
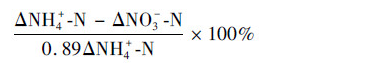
硝化作用去除的氨氮占比为:
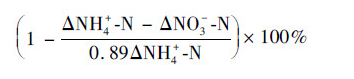
由此可对硝化和CANON作用去除的氨氮占比进行分析.
2.2.1 滤速对氨氮去除的影响分析
由2.1.4节分析知, 低温生物除铁锰硝化耦合CANON工艺在39 d时已经启动成功, 此时进水氨氮浓度为1.18 mg·L-1, 滤速为2 m·h-1, 出水氨氮浓度为0, 进出水亚氮浓度均为0, 进水硝氮浓度为0.11 mg·L-1, 出水硝氮浓度为1.06 mg·L-1, 故氨氮的去除量为1.18 mg·L-1, 硝氮变化量为0.95 mg·L-1, 氮素损失为0.23 mg·L-1, 由式(9)和(10)计算知, 经CANON过程去除的氨氮约为0.26 mg·L-1, 约占氨氮去除量的21.90%, 经硝化作用去除的氨氮约为0.92 mg·L-1, 约占氨氮去除量的78.10%.图 6为运行过程中CANON占比变化情况, 从中可知, 当平均进水氨氮浓度不变, 提高滤速会导致氨氮通过CANON过程去除的比例增加.且当进水氨氮浓度平均为1.2 mg·L-1, 滤速为2 m·h-1时, 氨氮的平均去除量为1.2 mg·L-1, CANON作用去除的氨氮平均约占氨氮去除量的22.28%, 约为0.27 mg·L-1, 故经硝化作用去除的氨氮平均约占氨氮去除量的77.72%, 约为0.93 mg·L-1; 当滤速提升至3 m·h-1时, 氨氮的平均去除量为1.2 mg·L-1, CANON作用去除的氨氮平均约占氨氮去除量的29.09%, 约为0.35 mg·L-1, 故经硝化作用去除的氨氮平均约占氨氮去除量的70.91%, 约为0.85 mg·L-1; 当滤速提升至4 m·h-1, 氨氮的平均去除量为1.2 mg·L-1, CANON作用去除的氨氮平均约占氨氮去除量的38.08%, 约为0.46 mg·L-1, 故经硝化作用去除的氨氮平均约占氨氮去除量的61.92%, 约为0.74 mg·L-1; 继续提升滤速至5 m·h-1, 氨氮的平均去除量仍为1.2 mg·L-1, CANON作用去除的氨氮平均约占氨氮去除量的44.95%, 约为0.54 mg·L-1, 故经硝化作用去除的氨氮平均约占氨氮去除量的55.05%, 约为0.66 mg·L-1.由此知, 当平均进水氨氮浓度为1.2 mg·L-1时, 提升滤柱运行滤速会导致通过CANON作用去除的氨氮及比例增加, 而通过硝化作用去除的氨氮及比例降低.具体联系污水宝或参见http://www.dowater.com更多相关技术文档。
当生物滤柱运行至70 d时, 进水氨氮浓度为1.73 mg·L-1, 滤速为3 m·h-1, 出水氨氮浓度为0, 进出水亚氮浓度均为0, 进水硝氮浓度为0.26 mg·L-1, 出水硝氮浓度为1.53 mg·L-1, 故氨氮的去除量为1.73 mg·L-1, 硝氮变化量为1.27 mg·L-1, 氮素损失为0.46 mg·L-1, 由式(9)和(10)知, 经CANON过程去除的氨氮约为0.52 mg·L-1, 约占氨氮去除量的29.88%, 经硝化作用去除的氨氮约为1.21 mg·L-1, 约占氨氮去除量的70.12%.由图 6可知, 当进水氨氮浓度平均为1.7 mg·L-1, 并以3 m·h-1的滤速运行时, 氨氮的平均去除量为1.7 mg·L-1, 经CANON过程去除的氨氮平均约占氨氮去除量的29.73%, 约为0.50 mg·L-1, 故经硝化作用去除的氨氮平均约占氨氮去除量的70.27%, 约为1.20 mg·L-1; 当滤速提升至4 m·h-1时, 氨氮的平均去除量为1.7 mg·L-1, CANON作用去除的氨氮平均约占氨氮去除量的35.99%, 约为0.61 mg·L-1, 故经硝化作用去除的氨氮平均约占氨氮去除量的64.01%, 约为1.09 mg·L-1; 继续提升滤速至5 m·h-1, 氨氮的平均去除量仍为1.7 mg·L-1, 经CANON作用去除的氨氮平均约占氨氮去除量的44.89%, 约为0.76 mg·L-1, 故经硝化作用去除的氨氮平均约占氨氮去除量的55.11%, 约为0.94 mg·L-1.由此知, 当进水氨氮浓度平均为1.7 mg·L-1时, 提升滤速会导致通过CANON作用去除的氨氮及比例增加, 而通过硝化作用去除的氨氮及比例降低.
当生物滤柱运行至105 d时, 进水氨氮浓度为2.22 mg·L-1, 滤速为3 m·h-1, 出水氨氮浓度为0, 进出水亚氮浓度均为0, 进水硝氮浓度为0.11 mg·L-1, 出水硝氮浓度为1.68 mg·L-1, 故氨氮的去除量为2.22 mg·L-1, 硝氮变化量为1.57 mg·L-1, 氮素损失为0.65 mg·L-1, 同样由式(9)和(10)知, 经CANON过程去除的氨氮约为0.73 mg·L-1, 约占氨氮去除量的32.90%, 经硝化作用去除的氨氮约为1.49 mg·L-1, 约占氨氮去除量的67.10%.结合图 6分析可知, 当滤柱以进水氨氮浓度平均为2.2 mg·L-1运行, 并在此浓度下梯次提升滤速, 当以3 m·h-1运行时, 氨氮的平均去除量为2.2 mg·L-1, 此时经CANON作用去除的氨氮平均约占氨氮去除量的32.45%, 约为0.71 mg·L-1, 经硝化作用去除的氨氮平均约占氨氮去除量的67.55%, 约为1.49 mg·L-1; 当提升至4 m·h-1, 氨氮的平均去除量仍为2.2 mg·L-1, 此时通过CANON作用去除的氨氮平均约占氨氮去除量的40.23%, 约为0.88 mg·L-1, 经硝化作用去除的氨氮平均约占氨氮去除量的59.77%, 约为1.32 mg·L-1; 继续提升滤速至5 m·h-1时, 氨氮的平均去除量降至约2.0 mg·L-1, CANON作用去除的氨氮平均约占氨氮去除量的45.75%, 约为0.92 mg·L-1, 经硝化作用去除的氨氮平均约占氨氮去除量的54.25%, 约为1.08 mg·L-1.因此, 当进水氨氮浓度平均为2.2 mg·L-1时, 提升滤速可能会降低氨氮的去除量, 但通过CANON作用去除的氨氮比例仍会增加, 而通过硝化作用去除的氨氮比例降低.
为进一步明确滤速对氨氮去除的影响, 笔者以进水氨氮浓度平均为2.2 mg·L-1时为例进行分析.图 7(a)为滤柱在102 d时沿程“三氮”变化情况, 图 7(b)为滤柱在115 d时沿程“三氮”变化情况, 其滤速分别为3 m·h-1和4 m·h-1.由图 7(a)知, 102 d时进水氨氮、亚氮和硝氮浓度分别为2.19、0和0.13 mg·L-1, 故进水总氮浓度为2.32 mg·L-1; 出水氨氮、亚氮和硝氮浓度分别为0、0和1.68 mg·L-1, 故出水总氮浓度为1.68 mg·L-1.此时氮素损失为0.64 mg·L-1, 由式(9)和(10)知, 经CANON过程去除的氨氮约为0.72 mg·L-1, 约占氨氮去除量的32.84%.由图 7(b)知, 115 d时进水氨氮、亚氮和硝氮浓度分别为2.18、0和0.15 mg·L-1, 故进水总氮浓度为2.33 mg·L-1; 出水氨氮、亚氮和硝氮浓度分别为0、0和1.55 mg·L-1, 故出水总氮浓度为1.55 mg·L-1.此时氮素损失为0.78 mg·L-1, 由式(9)和(10)可知, 经CANON过程去除的氨氮约为0.88 mg·L-1, 约占氨氮去除量的40.20%.故滤速由3 m·h-1提升至4 m·h-1时, 滤柱中经CANON过程去除的氨氮由0.72 mg·L-1增加至0.88 mg·L-1, 其占比由32.84%升高至40.20%.由此可进一步明确当进水浓度不变, 提升滤速会导致通过CANON过程去除的氨氮及比例增加, 而通过硝化作用去除的氨氮及比例降低.为明晰氨氮去除途径变化的原因, 笔者将继续以102 d和115 d时为例进行分析.
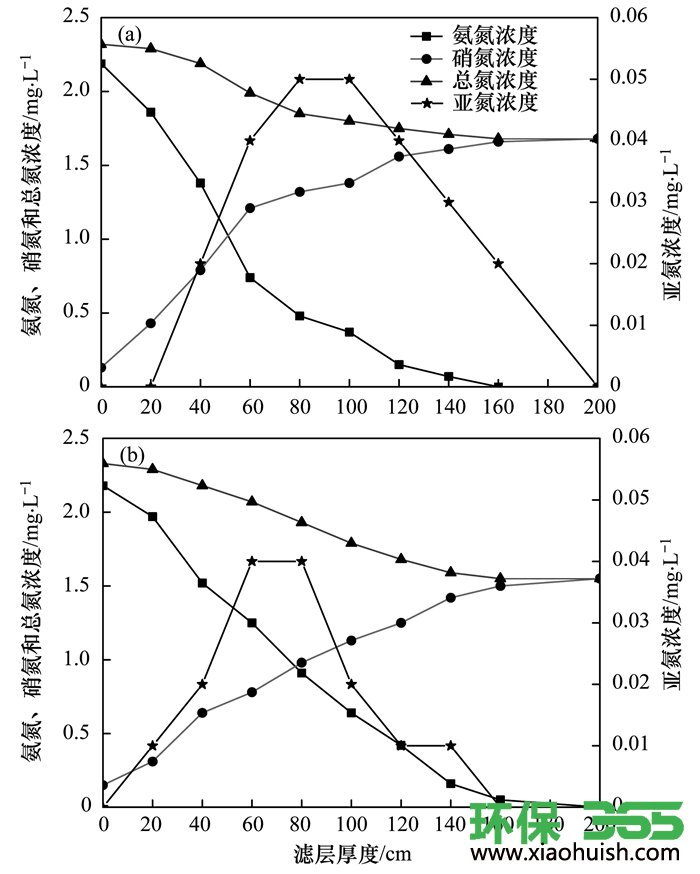
图 7 不同滤速时沿程“三氮”变化
由图 7(a)知, 在102 d以3 m·h-1运行时, 氨氮主要是在滤柱的前60 cm去除, 在60 cm处水中的氨氮为0.74 mg·L-1, 之后氨氮的去除速率明显降低, 在滤层20~200cm(出水)范围内的水中均有亚氮积累, 由总氮浓度沿程变化曲线知, 氮素损失主要发生在滤层的40~80 cm, 在此范围内共存有氨氮和亚氮, 符合CANON工艺所需的条件, 其可进一步说明硝化耦合CANON作用去除氨氮的过程已成功建立, 在之后的滤层中氮素损失量明显降低, 分析原因为:在此范围内虽存在亚氮和氨氮共存的现象, 但水中的氨氮浓度较低, 在滤层80 cm处水中的氨氮仅为0.47 mg·L-1, 导致此后滤层中CANON过程第二步所处的氨氮浓度降低, 进而导致此后滤层中通过CANON过程去除氨氮降低, 因此在此范围内氮素损失量降低.由图 7(b)知, 在115 d以4 m·h-1运行时, 滤柱中的亚氮在滤层的前160 cm范围内均有亚氮积累, 由总氮浓度沿程变化曲线知, 氮素损失主要发生在滤层的40~120 cm, 在此范围内亦共存有亚氮和氨氮, 同样满足CANON工艺所需的条件.在亚氮和氨氮共存的滤层中, 此时水中的氨氮浓度要高于3 m·h-1运行时的氨氮浓度, 尤其是在滤层60 cm之后, 60 cm处氨氮浓度为1.25 mg·L-1, 而3 m·h-1运行时60 cm处的氨氮浓度仅为0.74 mg·L-1, 两者浓度差距明显, 由图 7(b)中总氮浓度沿程变化曲线知, 此后滤层中仍有较高的氮素损失, 故此后滤层中的CANON作用仍较强.此外, 对比两者总氮浓度沿程变化曲线知, 在滤柱的前80 cm滤柱以3 m·h-1运行时的氮素损失速率大于滤柱以4 m·h-1运行的氮素损失速率, 而此后则反之, 造成此现象的原因可以由两者氨氮浓度沿程变化曲线进行说明:由氨氮浓度沿程变化曲线知, 滤柱以3 m·h-1运行时在滤层80 cm处的氨氮浓度仅为0.47 mg·L-1, 而滤柱以4 m·h-1运行时在滤层80 cm处的氨氮浓度为0.91 mg·L-1.低滤速时滤柱对氨氮及DO有较好的网捕效率, 且有较长的EBCT, 进水中的氨氮主要是在滤层上部去除, 氮素损失主要发生在滤层上部, 而提升滤速会导致滤柱的网捕能力和EBCT降低, 从而有更高浓度的氨氮进入滤层深处, 滤层深处的微生物能够接触到更多的氨氮离子, 导致滤层中CANON过程第二步所处的氨氮浓度升高, 提高了滤层深处AnAOB对氨氮离子的网捕效率, 微生物与氨氮浓度所处的动态平衡遭到破坏, 历经第一活性增长期, 滤层深处的ANAMMOX性能增强, 氮素损失速率增加.
由上述知, 当保持滤柱进水浓度不变, 提升滤速会使滤料表面的水流剪切力增大, 降低生物滤柱对氨氮等基质的网捕效率, 水中的氨氮向滤层深处位移, 增加了滤层深处的氨氮浓度, 氨氮和亚氮共存区域中氨氮的浓度得到提升, 因此提高了滤层深处AnAOB对氨氮离子的网捕效率, 增强了滤层深处的ANAMMOX性能.因此, 滤速增加会导致低温含铁锰氨地下水中通过CANON作用去除的氨氮增加, 而通过硝化作用去除的氨氮降低.
2.2.2 水质对氨氮去除的影响分析
在该生物滤柱中当进水氨氮浓度平均分别为1.2 mg·L-1和1.7 mg·L-1时, 平均进水DO浓度约为8.3 mg·L-1, 当进水氨氮浓度平均为2.2 mg·L-1时, 平均进水DO浓度调整为约10.0 mg·L-1.由表 2及图 6分析知, 当滤柱均以3 m·h-1运行, 平均进水氨氮浓度为1.2 mg·L-1时, 平均的去除氨氮量为1.2 mg·L-1, 平均出水DO浓度约为2.70 mg·L-1, 经CANON过程去除的氨氮约为0.35 mg·L-1, 约占氨氮去除量的29.09%, 经硝化作用去除的氨氮约为0.85 mg·L-1, 约占氨氮去除量的70.91%;当平均进水氨氮浓度为1.7 mg·L-1时, 平均的氨氮去除量为1.7 mg·L-1, 平均出水DO浓度约为1.17 mg·L-1, CANON作用去除的氨氮约为0.5 mg·L-1, 约占氨氮去除量的29.73%, 硝化作用去除的氨氮约为1.20 mg·L-1, 约占氨氮去除量的70.27%;当平均进水氨氮浓度为2.2 mg·L-1, 此时平均的氨氮去除量为2.2 mg·L-1, 平均出水DO浓度约为0.72 mg·L-1, 经CANON过程去除的氨氮约为0.71 mg·L-1, 约占氨氮去除量的32.45%, 经硝化作用去除的氨氮约为1.49 mg·L-1, 约占氨氮去除量的67.55%.当滤柱均以4 m·h-1运行, 进水氨氮浓度平均为1.2 mg·L-1时, 氨氮的平均去除量为1.2 mg·L-1, 平均出水DO浓度约为2.98 mg·L-1, 经CANON过程去除的氨氮约为0.46 mg·L-1, 约占氨氮去除量的38.08%, 经硝化作用去除的氨氮约为0.74 mg·L-1, 约占氨氮去除量的61.92%;当进水氨氮浓度平均为1.7 mg·L-1时, 氨氮的平均去除量为1.7 mg·L-1, 平均出水DO浓度约为1.43 mg·L-1, 经CANON过程去除的氨氮约为0.61 mg·L-1, 约占氨氮去除量的35.99%, 经硝化作用去除的氨氮约为1.09 mg·L-1, 约占氨氮去除量的64.01%;当进水氨氮浓度平均为2.2 mg·L-1时, 氨氮的平均去除量为2.2 mg·L-1, 平均出水DO浓度约为1.13 mg·L-1, 经CANON过程去除的氨氮约为0.88 mg·L-1, 约占氨氮去除量的40.23%, 经硝化作用去除的氨氮约为1.32 mg·L-1, 约占氨氮去除量的59.77%.当滤柱均以5 m·h-1运行, 进水氨氮浓度平均为1.2 mg·L-1时, 氨氮的平均去除量为1.2 mg·L-1, 平均出水DO浓度约为3.19 mg·L-1, 经CANON过程去除的氨氮约为0.54 mg·L-1, 约占氨氮去除量的44.95%, 经硝化作用去除的氨氮约为0.66 mg·L-1, 约占氨氮去除量的55.05%;当平均进水氨氮浓度为1.7 mg·L-1时, 平均去除的氨氮为1.7 mg·L-1, 出水DO浓度平均约为1.82 mg·L-1, CANON过程去除的氨氮约为0.76 mg·L-1, 约占氨氮去除量的44.89%, 硝化作用去除的氨氮约为0.94 mg·L-1, 约占氨氮去除量的55.11%;当平均进水氨氮浓度为2.2 mg·L-1时, 平均的氨氮去除量降至约2.0 mg·L-1, 平均出水DO浓度约为2.14 mg·L-1, 经CANON过程去除的氨氮约为0.92 mg·L-1, 约占氨氮去除量的45.75%, 经硝化作用去除的氨氮约为1.08 mg·L-1, 约占氨氮去除量的54.25%.故由上述知, 当滤速保持不变, 适度提升进水氨氮浓度, 会导致通过CANON作用去除的氨氮增加.为进一步明确水质对氨氮去除的影响, 笔者将以运行滤速均为4 m·h-1, 平均进水氨氮浓度分别为1.2和1.69 mg·L-1为例进行分析.
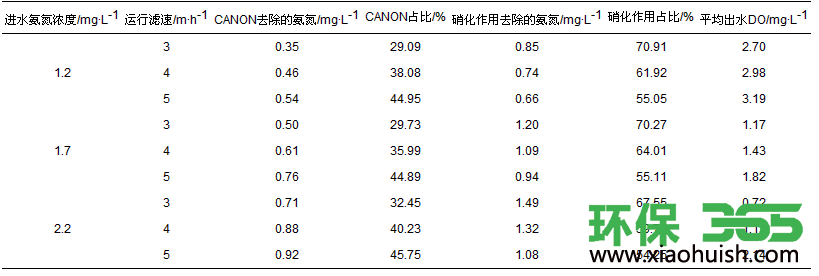
表 2 不同条件下氨氮的去除途径
图 8(a)为57 d时的沿程“三氮”变化, 图 8(b)为80 d时的沿程“三氮”变化.由表 1成熟滤料吸附实验知, 27 d时滤料已经吸附饱和, 可以忽略其对氨氮转化去除的影响, 生物滤柱中总氮损失仅是由于CANON过程造成的.由图 8(a)可知, 57 d时进水氨氮、亚氮和硝氮的浓度分别为1.21、0和0.21 mg·L-1, 进水总氮浓度为1.42 mg·L-1; 出水氨氮、亚氮和硝氮的浓度分别为0、0和1.02 mg·L-1, 出水总氮浓度为1.02 mg·L-1, 由此可知, 氮素损失为0.4 mg·L-1, 由式(9)和(10)可知, 经CANON过程去除的氨氮约为0.45 mg·L-1, 出水DO浓度约为2.88 mg·L-1.由图 8(b)可知, 80 d时进水氨氮、亚氮和硝氮的浓度分别为1.69、0和0.13 mg·L-1, 进水总氮浓度为2.33 mg·L-1; 出水氨氮、亚氮和硝氮的浓度分别为0、0和1.27 mg·L-1, 出水总氮浓度为1.27 mg·L-1, 故氮素损失为0.55 mg·L-1, 同样由式(9)和(10)可知, 经CANON过程去除的氨氮约为0.62 mg·L-1, 此时出水DO浓度约为1.51 mg·L-1较57 d时有明显降低, 而通过CANON作用去除的氨氮明显增加.为明晰氨氮通过CANON作用去除量增加的原因, 笔者仍将以57 d和80 d时为例进行分析.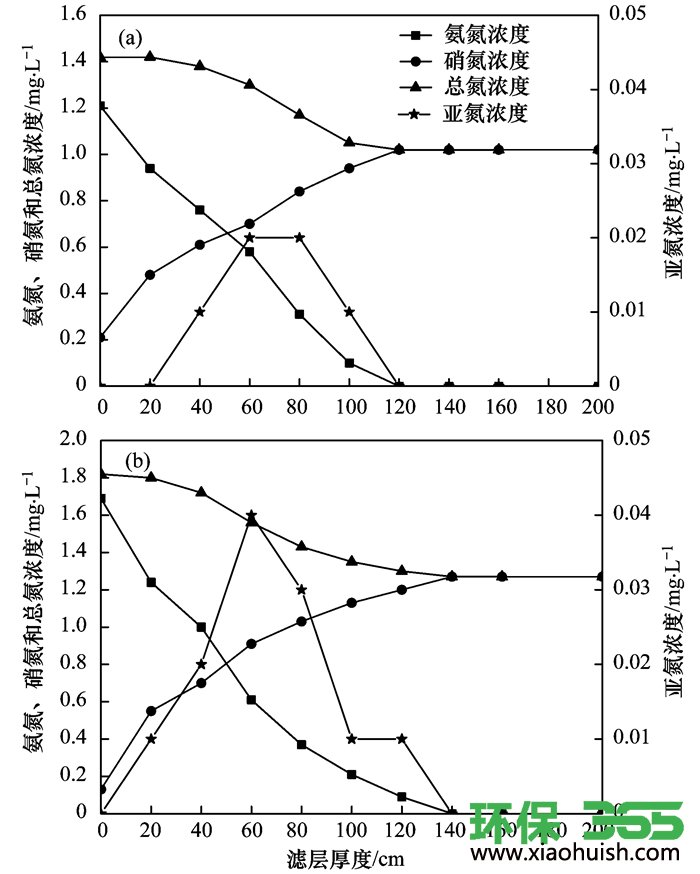
图 8 不同浓度时沿程“三氮”变化
由图 8(a)知, 当进水氨氮浓度为1.21 mg·L-1时, 滤柱中的氨氮至滤层120 cm处降低至0, 在滤层20 cm至120 cm范围内的水中均有亚氮积累, 由总氮浓度沿程变化曲线知, 氮素损失主要发生在滤层的40~100 cm, 在滤层40~100 cm范围内共存有亚氮和氨氮, 满足CANON工艺的条件.而由图 8(b)知, 当进水氨氮浓度提升至1.69 mg·L-1时, 滤柱中的氨氮需至滤层140 cm处降低至0, 对比57 d时进水氨氮浓度为1.21 mg·L-1可知, 进水氨氮浓度增加会导致氨氮去除区位向滤层深处位移, 此时在滤层前140 cm的水中均有亚氮积累, 同样由总氮浓度沿程变化曲线知, 氮素损失主要发生在滤层的20~120 cm, 在滤层20~120 cm范围内亦共存亚氮和氨氮, 同样满足CANON工艺所需的条件.由上文已知, 当进水氨氮浓度为1.21 mg·L-1时, 经CANON过程去除的氨氮约为0.45 mg·L-1, 而当进水氨氮浓度为1.69 mg·L-1时, 经CANON过程去除的氨氮增加至0.62 mg·L-1.相较于前者, 后者经CANON过程去除的氨氮增加的原因亦可以由两者的氨氮浓度沿程变化曲线进行说明:由氨氮浓度沿程变化曲线和亚氮浓度沿程变化曲线知, 滤柱在57 d以进水氨氮浓度为1.21 mg·L-1运行时在氨氮和亚氮共存区域中的氨氮浓度要小于滤柱在80 d以进水氨氮浓度为1.69 mg·L-1运行时在氨氮和亚氮共存区域中的氨氮浓度, 故后者滤层中CANON过程第二步所处的氨氮浓度升高, 提高了滤层中AnAOB对氨氮离子的网捕效率, 微生物与氨氮浓度所处的动态平衡遭到破坏, 历经第一活性增长期, 滤层的ANAMMOX性能增强.因此保持滤速不变, 提升进水氨氮浓度会导致通过CANON作用去除的氨氮增加.
综上所述, 当保持滤速不变, 提升进水氨氮浓度会使更高浓度的氨氮进入滤层, 增加了滤层深处的氨氮浓度, 在氨氮和亚氮的共存区域中氨氮的浓度得到提升, 提高了滤层中AnAOB对氨氮离子的网捕效率, 增强了滤层的ANAMMOX性能.因此, 保持滤速不变, 提升进水氨氮浓度会导致通过CANON作用去除的氨氮增加.
3 结论
(1) 保持滤柱进水浓度不变, 提升滤速会导致低温(6~8℃)含铁锰氨[Fe(Ⅱ) 2.91~6.35 mg·L-1、Mn(Ⅱ) 0.47~0.98 mg·L-1和NH4+-N 1.15~2.26 mg·L-1]地下水中CANON作用增强, 而硝化作用减弱.
(2) 保持滤柱运行滤速不变, 提升进水氨氮浓度会导致低温(6~8℃)含铁锰氨[Fe(Ⅱ) 2.91~6.35 mg·L-1、Mn(Ⅱ) 0.47~0.98 mg·L-1和NH4+-N 1.15~2.26 mg·L-1]地下水中通过CANON作用去除的氨氮增加.(来源:北京工业大学水质科学与水环境恢复工程北京市重点实验室 作者:张杰)
三六五环保是深圳、广州、佛山、珠海、中山、江门等珠三角地区专业的回收销毁公司,深圳文件销毁公司,电子产品销毁公司,过期食品销毁公司,过期化妆品销毁公司,电脑硬盘销毁公司,保密资料销毁公司,服装销毁公司,假冒伪劣产品销毁公司,不合格产品销毁公司,平台运作及服务中心设。
上海金山生活污水处理企业可信吗?
上海金山365污水污泥处理公司 : 是长期专注于食品、饮料领域。本公司倡导“专业、务实、高效、创新”的企业精神,具有良好的内部机制。优良的工作环境以及良好的激励机制,吸引了一批高素质、高水平、高效率的人才。拥有完善的技术研发力量和成熟的售后服务团队。我们的宗旨是:“用服务与真诚来换取你的信任与支持,互惠互利,共创双赢!”我公司愿与国内外各界同仁志士竭诚合作,共创未来!主要业务:污水处理 污泥处理、生活污水处理、污泥回收、污泥处置、城市污水处理、污水污泥处理、污泥干燥、废水处理、活性污泥处理、污泥处理工艺、活性污泥处理、含油污泥处理、工业污泥处理、工业污水处理、城市污泥处理、农村污水处理、食品污水处理等服务。